IDENTYFIKACJA SSc‑ILD WYMAGA WYSOKIEGO POZIOMU CZUJNOŚCI, PONIEWAŻ NIE U WSZYSTKICH PACJENTÓW WYSTĘPUJĄ OBJAWY ODDECHOWE6
Najczęstsze początkowe objawy SSc-ILD to uczucie zmęczenia, duszność wysiłkowa i suchy kaszel, choć wczesna SSc-ILD często przebiega bezobjawowo.7 Uwzględnianie jedynie obecności lub nasilenia objawów ze strony układu oddechowego, np. duszności wysiłkowej, przy określaniu częstości występowania zajęcia płuc może skutkować przeoczeniem rozpoznania u dużej mniejszości pacjentów z SSc-ILD z łagodną chorobą śródmiąższową.8 U pacjentów z SSc z „ciężką” chorobą płuc objawy płucne często rozwijają się dopiero po wystąpieniu znacznego spadku FVC, nawet jeśli wartość FVC jest nieprawidłowa już podczas oceny wyjściowej i/lub zmniejsza się z czasem, niezależnie od tego, czy występują objawy.9
W badaniu przedmiotowym, oprócz objawów skórnych związanych z SSc, zwykle stwierdza się trzeszczenia typu „taśmy rzepowej” w badaniu osłuchowym płuc.10
Najczęstsze objawy przedmiotowe i podmiotowe SSc‑ILD*
| Objawy podmiotowe SSc‑ILD | Objawy przedmiotowe SSc‑ILD |
* Wczesna SSc-ILD może przebiegać bezobjawowo.13,15
U PACJENTÓW Z SSc NALEŻY WYKONAĆ WYJŚCIOWO PRZESIEWOWE BADANIE HRCT PŁUC POD KĄTEM ILD1,2,5
U pacjentów z SSc należy wykonać dokładną ocenę kliniczną, w tym badanie obrazowe klatki piersiowej metodą HRCT, PFT, DLCO i badanie osłuchowe, aby zapewnić wczesną identyfikację ILD i uzyskać wartości wyjściowe do porównywania z przyszłymi wynikami.1,4,6,13
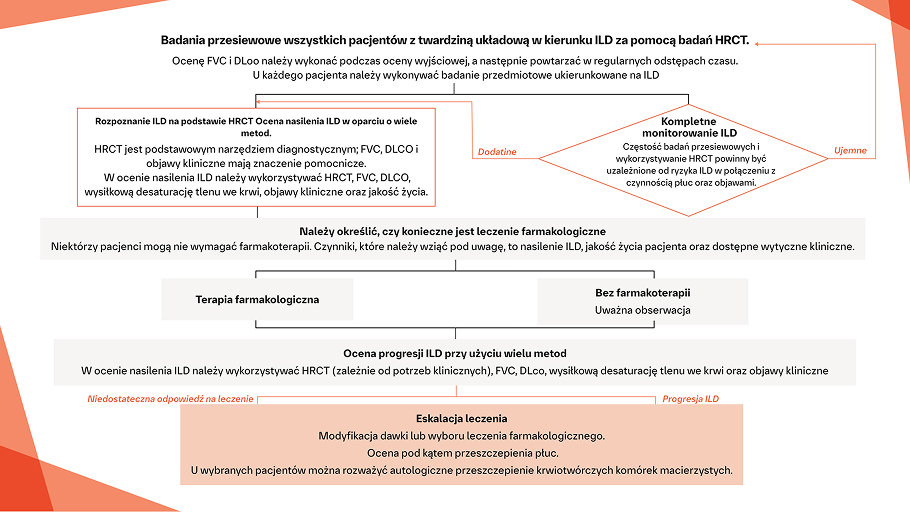
Ocena przesiewowa i algorytm diagnostyczny w SSc‑ILD1
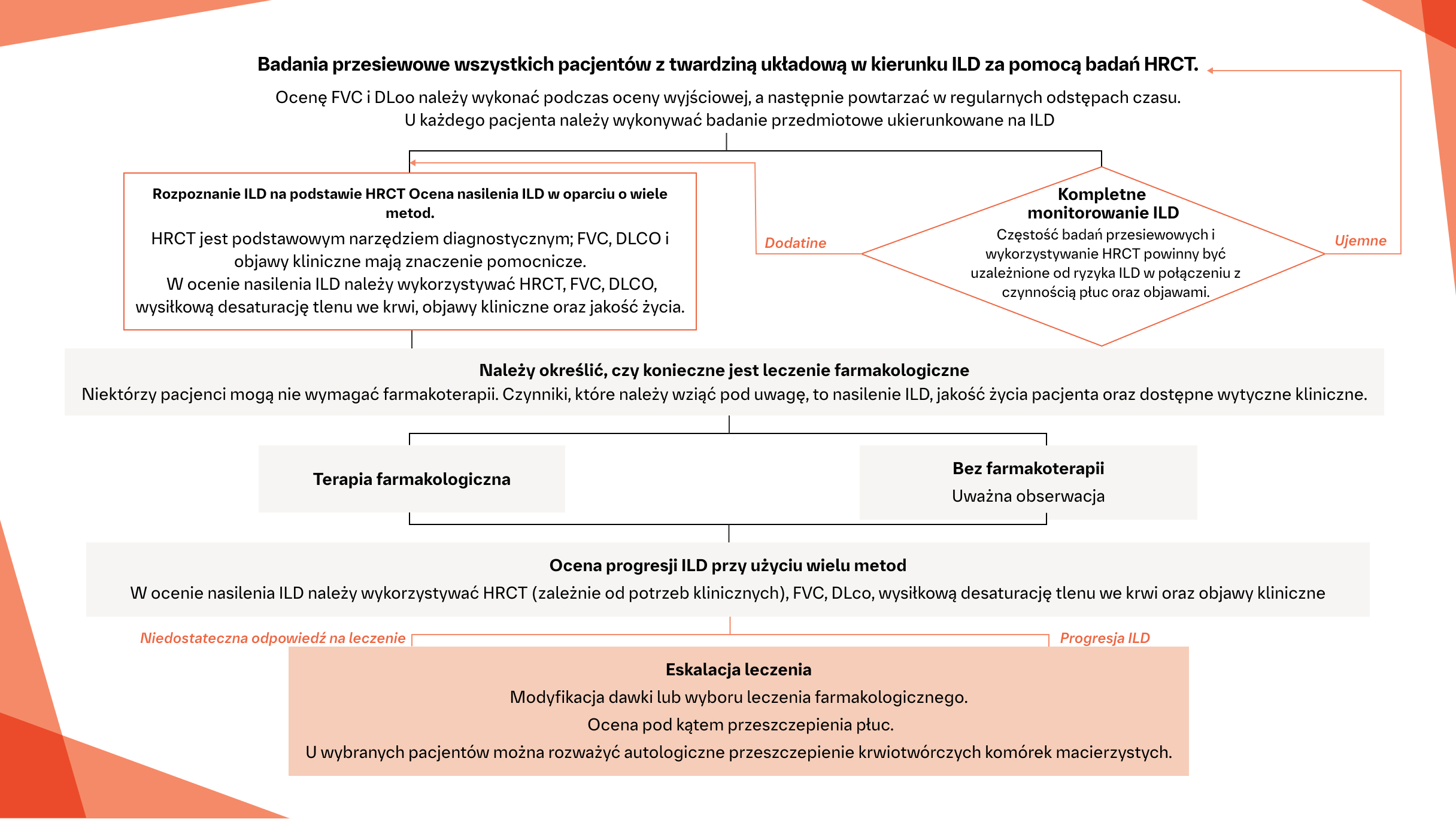
Algorytm ten zawiera krótkie podsumowanie konsensusu europejskiego opartego na dowodach, z uwzględnieniem uzupełniającego procesu Delphi, na podstawie opinii ekspertów z komitetu sterującego, w odniesieniu do identyfikacji i postępowania w SSc-ILD – do wykorzystania w praktyce klinicznej.
Na podstawie: Hoffmann-Void AM, et al. Lancet Rheum.2020;2:e71-e83.
Opieranie się na PFT jako jedynej metodzie oceny przesiewowej pod kątem SSc-ILD może powodować, że klinicyści będą przeoczali znaczną liczbę pacjentów, biorąc pod uwagę wysoki odsetek wyników fałszywie ujemnych.9,13 Wartość badań PFT jako metody przesiewowej jest ograniczona ze względu na szerokie zakresy prawidłowe PFT (np. 80–120% średniej wartości odnotowanej w dobranych pod względem wieku oraz płci populacjach referencyjnych), co może utrudniać interpretację danych przesiewowych.14
Ryzyko wczesnego zgonu z powodu ILD18,19 podkreśla znaczenie podstawowych badań przesiewowych w kierunku ILD u pacjentów z SSc.1,5
Włóknienie płuc stanowi główną przyczynę zgonów w SSc, odpowiadając za ~35% zgonów związanych z tą chorobą15,16
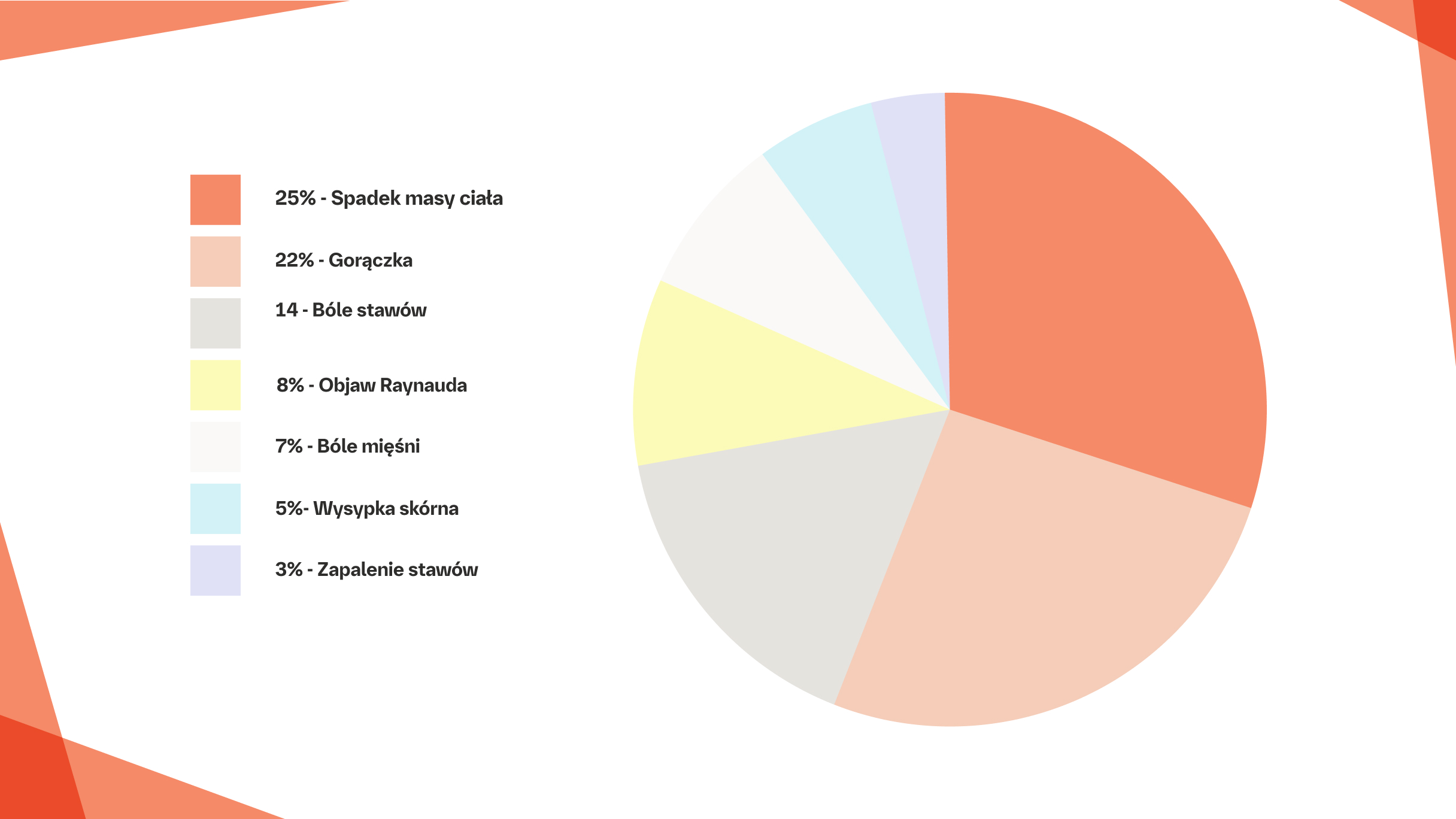
Przyczyny zgonów związanych z SSc (1997–2001).
Na podstawie: Steen VD and Medsger TA. Ann Rheum Dts. 2007;66:940-944 and Tyndall AJ. et al. Ann Rheum Dts. 2010:69(10):1809-1815.

Jak można ustalić rozpoznanie SSc-ILD?
Jak należy postępować z pacjentem z SSc‑ILD po ustaleniu rozpoznania?
w przebiegu SSc
Leczenie SSc‑ILD
postępowania

Ciągłe monitorowanie
w SSc‑ILD
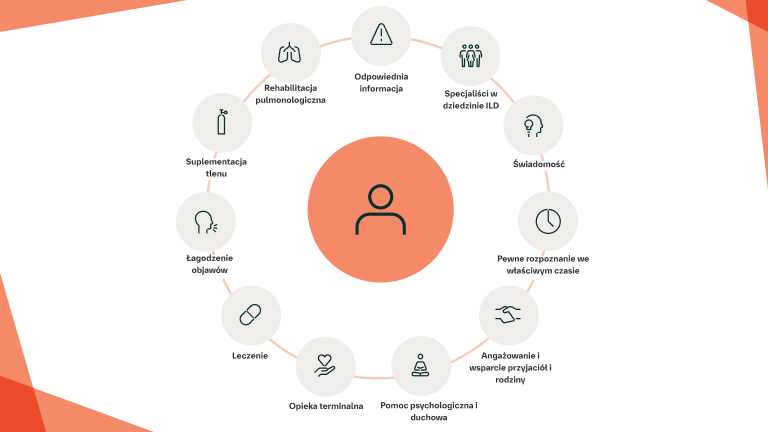
Zapewnienie opieki paliatywnej/wspomagającej
Przypisy
-
CTD-ILD: śródmiąższowa choroba płuc związana z chorobą tkanki łącznej; DLCO: pojemność dyfuzyjna płuc dla tlenku węgla; FVC: natężona pojemność życiowa; HRCT: tomografia komputerowa wysokiej rozdzielczości; ILD: śródmiąższowa choroba płuc; PFT: badania czynnościowe płuc; SSc: twardzina układowa; SSc-ILD: śródmiąższowa choroba płuc związana z twardziną układową.
-
Hoffmann-Vold AM, Maher TM, Philpot EE, et al. The identification and management of interstitial lung disease in systemic sclerosis: evidence-based European consensus statements. Lancet Rheum. 2020;2 e71–e83.
-
Asano Y, Jinnin M, Kawaguchi Y, et al. Diagnostic criteria, severity classification and guidelines of systemic sclerosis: Guideline of SSc. J Dermatol. 2018;45;633–691.
-
Denton CP, Khanna D. Systemic sclerosis. Lancet. 2017;390;1685–1699.
-
Roofeh D, Jaafar S, Vummidi D, et al. Management of systemic sclerosis-associated interstitial lung disease. Curr Opin Rheumatol. 2019;31;241–249.
-
Hoffmann-Vold AM, Fretheim H, Halse AK, et al. Tracking impact of interstitial lung disease in systemic sclerosis in a complete nationwide cohort. Am J Respir Crit Care Med. 2019;200;1258–1266.
-
Cottin V, Brown KK. Interstitial lung disease associated with systemic sclerosis (SSc-ILD). Respir Res. 2019;20:13.
-
Volkmann ER, Tashkin DP. Treatment of systemic sclerosis–related interstitial lung disease: a review of existing and emerging therapies. Annals ATS. 2016;13:2045–2056.
-
Wells AU. Interstitial lung disease in systemic sclerosis. La Presse Médicale. 2014;43:e329–e343.
-
Chowaniec M, Skoczyńska M, Sokolik R, et al. Interstitial lung disease in systemic sclerosis: challenges in early diagnosis and management. Reumatologia. 2018;56:249–254.
-
Perelas A, Silver RM, Arrossi AV, et al. Systemic sclerosis-associated interstitial lung disease. Lancet Respir Med. 2020;8;304–320.
-
Herzog EL, Mathur A, Tager AM, et al. Review: interstitial lung disease associated with systemic sclerosis and idiopathic pulmonary fibrosis: How similar and distinct?: SSc-Associated ILD and IPF. Arthritis Rheumatol. 2014;66;1967–1978.
-
Distler O, Assassi S, Cottin V, et al. Predictors of progression in systemic sclerosis patients with interstitial lung disease. Eur Respir J. 2020;55;1902026.
-
Hoffmann-Vold A, Aaløkken TM, Lund MB, et al. Predictive Value of Serial High-Resolution Computed Tomography Analyses and Concurrent Lung Function Tests in Systemic Sclerosis. Arthritis Rheumatol. 2015;67:2205–2212.
-
Molberg Ø, Hoffmann-Vold AM. Interstitial lung disease in systemic sclerosis: progress in screening and early diagnosis. Curr Opin Rheumatol. 2016;28:613–618.
-
Steen VD, Medsger TA. Changes in causes of death in systemic sclerosis, 1972-2002. Ann Rheum Dis. 2007;66:940–944.
-
Tyndall AJ, Bannert B, Vonk M, et al. Causes and risk factors for death in systemic sclerosis: a study from the EULAR Scleroderma Trials and Research (EUSTAR) database. Ann Rheum Dis. 2010;69:1809–1815.
-
Hoffmann-Vold AM, Allanore Y, Alves M, et al. Progressive interstitial lung disease in patients with systemic sclerosis-associated interstitial lung disease in the EUSTAR database. Ann Rheum Dis. 2020;217455.
-
Distler O, Volkmann ER, Hoffmann-Vold AM, et al. Current and future perspectives on management of systemic sclerosis-associated interstitial lung disease. Expert Rev Clin Immunol. 2019;15:1009–1017.
-
Ryerson CJ, Cayou C, Topp F, et al. Pulmonary rehabilitation improves long-term outcomes in interstitial lung disease: a prospective cohort study. Respir Med. 2014;108(1):203-210.
-
Kreuter M, Bendstrup E, Russell A, et al. Palliative care in interstitial lung disease: living well. Lancet Respir Med. 2017;5(12):968-980.
-
Maher TM, Wuyts W. Management of Fibrosing Interstitial Lung Diseases. Adv Ther. 2019;doi:10.1007/s12325-019-00992-9. [Epub ahead of print].
-
Sgalla G, Cerri S, Ferrari R, et al. Mindfulness-based stress reduction in patients with interstitial lung diseases: a pilot, single-centre observational study on safety and efficacy. BMJ Open Respir Res. 2015;2(1):e000065.
Materiały dla pacjentów po angielsku





